Super GelRed ® 核酸凝胶染料 10,000
Super GelRed ® 是一种高灵敏、无毒超安全和超稳定的
荧光核酸凝胶染色试剂(在工作浓度中)。它可替代溴化乙
锭 (EtBr,EB),具有远高于 EB 的灵敏度,同时不需要脱
色。由于 Super GelRed ® 和 EB 有相同的光谱特性,因此用
它替代 EB 时不需要更换成像系统
- 描述
- 常见问题
- 常见问答
描述
Super GelRed ® 核酸凝胶染料 10,000 ×
产品货号:S2001 ( in water ) S2002 ( in DMSO )
产品规格:0.5 mL
储存条件:避光,室温保存
产品介绍
Super GelRed ®是一种高灵敏、无毒超安全和超稳定的荧光核酸凝胶染色试剂(在工作浓度中)。它可替代溴化乙锭 (EtBr,EB),具有远高于 EB 的灵敏度,同时不需要脱色。由于 Super GelRedr 和 EB 有相同的光谱特性,因此用它替代 EB 时不需要更换成像系统。
使用方法
1 .胶染法(用法同 EB )
(1)制胶时加入 Super GelRed ® 核酸染料
(例如:每 50 mL 琼脂糖溶液中加入 5 μL Super GelRed ®10,000× 储液,以此比例类推)。
(2)按照常规方法进行电泳。
注意事项:
此方法染色染料用量相对较少,500 μL 染料大约可以做 100 块 50 mL 的胶。
由于 Super GelRed ® 具有良好的热稳定性,可以在热的琼脂糖溶液中直接添加,而不需要等待溶液冷却。摇晃,振荡或者翻转以保证染料充分混匀。也可以选择将 Super GelRed ® 储液加到含有琼脂糖粉末的电泳缓冲液中,然后用微波炉或其他常用方式加热以制备琼脂糖凝胶。Super GelRed ® 兼容所有常用的电泳缓冲溶液。
2 .泡染法
(1)按照常规方法进行电泳。
(2)用 H 2 O 将 Super GelRed ® 10,000× 储液稀释约 3,300倍到 0.1 M NaCl 中,制成 3× 染色液。(例如将 15 μL Super GelRed ® 10,000× 储液,5 mL 1 M NaCl加到45 mL H 2 O 中)。
(3)将凝胶小心地放入合适的容器中,如聚丙烯容器中,缓慢加入足量的 3× 染色液浸没凝胶,室温振荡染色 30 min左右,即可获得理想的效果。最佳染色时间根据凝胶厚度以及琼脂糖浓度不同而略有不同。对于含 3.5~10%丙烯酰胺的凝胶,染色时间通常介于 30 min 到 1 h,并随丙烯酰胺含量增加而延长。
强烈推荐:为了缩短泡染时间,染色液可以预先加热至 70℃左右,然后放入凝胶,孵育 10min 即可获得理想的效果。具体步骤见下页使用说明。
注意事项:
用泡染法染色时,染料用量较多,单次使用的染色液可重复使用 3 次左右。3× Super GelRed ® 染色液可以大量制备,在室温下避光保存直至用完。
注:1. 如果总是看到条带弥散或分离不理想,建议使用泡染法染色以确认问题是否与染料有关。
2. 如果染色后问题依旧存在,则说明问题与染料无关,请尝试:降低琼脂糖浓度、选用更长的凝胶、延长凝胶时间以保证边缘清晰、改进上样技巧或选择泡染法染色。
Super GelRed ® EB
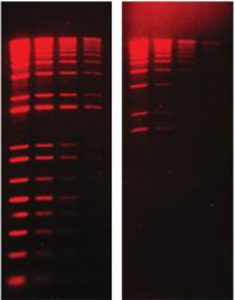
图一. Super GelRed ® 、EB 胶染法电泳效果对比
(1% Agar 凝胶在 1×TBE 缓冲液中电泳,1kb DNA ladder 上样量分别为:200ng, 100ng, 50ng, 25ng,使用 302nm激发的紫外凝胶成像仪拍照。)
一、实验目的
核酸的琼脂糖凝胶电泳实验,对核酸(DNA 或 RNA)进行分离、鉴定和纯化等分析。
二、主要试剂
1. 琼脂糖(如 US Everbright A2015)
2. 1×TBE 电泳缓冲液
3. 0.1 M 的 NaCl 水溶液
4. DNA Marker: 如 US Everbright 1kb DNA ladder (DL2031)
5. 10000× Super GelRed ® in water/DMSO(S2001/2002)
三、实验方案
1. 根椐制胶量及凝胶浓度,准确称量琼脂糖粉(如 1%的凝胶,即 1 g 琼脂糖加入 100 mL 1× TBE)。
2. 加入一定量的 1× TBE 电泳缓冲液(总液体量不宜超过锥形瓶的 50%容量)
注:用于电泳的缓冲液和用于制胶的缓冲液必须一致。
3. 锥形瓶在微波炉中加热,溶化琼脂糖。此操作重复 2-3次,直至琼脂糖完全溶化,形成均一、透明溶液。
4.根据实验需要,采用胶染法或者泡染法,两种方法选择一种即可:
1) 胶染法(用法同 EB):琼脂糖溶液加入 10000× Super GelRed ® 核酸染料。每 50 mL 胶中加入 5 μL Super GelRed ®核酸染料,并充分混匀,将凝胶溶液倒入制胶模中,然后在适当位置处插上梳子,在室温下使胶凝固(大约 30 min~1 h)。
(由于 Super GelRed ® 具有出色的热稳定性,可将试剂直接加入高温的凝胶溶液中,无需等待凝胶溶液冷却后再加入。也可采用将 Super GelRed ® 试剂预先与含有琼脂糖粉末的TBE 溶液混合,加热制成)。
2) 泡染法:直接将不含有 Super GelRed ® 染料的琼脂糖溶
液倒入制胶模中,然后在适当位置处插上梳子,在室温下使
胶凝固(大约 30 min~1 h)。
5. 将做好的凝胶放置于电泳槽中,上样。
6. 电泳:在 1× TBE 的电泳缓冲液中,100-120 V 电泳 45-90
min(电泳时间视具体情况而定)。
7. 1) 胶染法:直接图像采集,通过标准的透视器(302 nm)
观察染色凝胶,拍照、保存。
2) 泡染法:用 0.1 M 的 NaCl 水溶液按照 3300﹕1 的比例稀释 Super GelRed ® 浓缩液,混匀,制成 3× Super GelRed ®染色溶液,将染色溶液倒入合适的聚丙烯容器中,放入凝胶,缓慢加入足量的 3× 染色溶液浸没凝胶,室温轻轻振荡染色30 min 左右,具体染色时间因凝胶浓度和厚度而定。
强烈推荐:为了缩短泡染时间,染色液可以预先加热,然后放入凝胶,温育 10min 即可获得理想的效果。加热方式可采用水浴法或微波加热法,具体步骤如下:
a. 水浴加热法:将配制的 3× Super GelRed ® 染色液放入70~75℃的水浴锅中预热,然后将电泳凝胶小心放入上述预热的染色液中,在水浴锅中水浴加热 5~10min左右(泡染期间可以间隔轻摇几次,加速染料与核酸的结合)。
b. 微波加热法:将电泳结束后的凝胶放入配制的 3×Super GelRed ® 染色液中,放入微波炉中加热,先加热约 30s,取出泡染装置,摇床孵育 30s-1min,待染液温度下降后,再微波加热 10~15s,然后摇床孵育,重复上述步骤 4-5 次 (注意微波加热时间不可过长,防止琼脂糖凝胶溶化)。
8. 图像采集:通过标准的透视器(302 nm)观察染色凝胶,拍照、保存。(染色溶液可重复使用 2-3 次。如果不是立即再用的话,建议将用过的染色溶液 4 度保存。)
四、注意事项:
1. 鉴于 Super GelRed ® 的高灵敏性,建议减少 DNA 的上样量,推荐已知浓度样品的上样量为 50-200 ng/泳道(8 泳道的小胶孔),对于未知浓度的样品,尝试 1/3 或 1/5 的常用上样量。根据胶孔大小适当增加或降低上样量。
2. 使用胶染法时,经检测 Super GelRed ® 跟市面上的一些DNA Ladder 存在不匹配的现象,如 Takara、天根的 marker,条带分离效果不佳,因此我们推荐使用的 marker 品牌有 US Everbright、Promega、Vazyme。
3. 推荐用 1×TBE 缓冲液代替 TAE,因为含硼酸盐的试剂导电性更好。电泳时电压不宜过高,一般TBE不要超过120V,TAE 不要超过 100 V。
4. 染料无需低温冷藏,请于室温下储存,以避免沉淀,若发现沉淀,请将染料加热至 45-50℃,2 min,振荡溶解,不影响使用效果。
推荐:聚丙烯酰胺凝胶核酸电泳推荐使用我司 S2005 SuperPage GelRed ® 染料,效果更佳。
| 问题 | 建议 |
| 胶染法中 DNA 条带弥散,拖尾 | 1.将 DNA 上样量减少至三分之一或五分之一。Super GelRed ® 比 EB 更加灵敏,条带的弥散或拖尾可能是超载造成的。这是 DNA ladder 的常见现象,推荐使用我司提供的与 Super GelRed ® 匹配性较好的 DNA ladder。 2.用泡染法(后染)代替胶染法(前染)。 3.使用低浓度的琼脂糖凝胶检测大片段 DNA。 4.更换电泳缓冲液,TBE 缓冲液比 TAE 缓冲液的效果好。 5.loading buffer 含有 SDS 可能会引起条带的弥散和拖尾,如果发生这种情况,建议使用泡染法 |
| 胶染法中 DNA 迁移率的差异 | 由于 Super GelRed ® 的分子量较大,导致其不能进入细胞,保证了染料的安全性。但是,大分子量导致 DNA 的迁移速率可能会受到染料与 DNA 比率的影响。 1. 将 DNA 上样量减少至三分之一或五分之一。 2. 使用泡染法,避免染料在电泳过程中对迁移造成干扰。 |
| 荧光较弱,一段时间后染料性能 降低,或使用后染法染色不均匀 | 染料可能在溶液中已沉淀。 1. 加热 Super GelRed ® 至 45-50℃,2min,涡旋溶解。 2. 染料在室温下储存,避免沉淀。 |
| Qubit dsDNA 标准液 2 (组分 D) | 2-6ºC |
| 常见问答 | 回答 |
| Super GelRed ® 是否可用于单链 DNA 或 RNA 染色? | Super GelRed ® 可以用来染色单链 DNA 和 RNA,但是它对双链 DNA 的灵 敏度是单链 DNA 或 RNA 的五倍。 |
| Super GelRed ® 与哪些 loading buffer 兼容? | 我们通常使用含有 15% glycerol, 7.5% Ficoll 400, 0.05% Bromophenol Blue, and 0.1% Patent Blue VF 的 6× loading buffer。在内部测试中,包含 0.1% Orange G 的 6X loading buffer 在 Super GelRed ® 的前染和后染中都有良好 的效果, loading buffer 中的 SDS 可能会造成 Super GelRed ® 的前染中条带 的弥散和拖尾。如果出现这种情况,我们建议使用后染法。 |
| Super GelRed ® 预制凝胶跑完电泳 后是否可以重复使用? | Super GelRed ® 预制凝胶可重复使用 2-3 次,但我们不建议客户重复使用, 因为这会降低后续电泳的信号强度。 |
| Super GelRed ® 该如何处理掉? | Super GelRed ® 已被相关部门批准可直接倒进下水道。但是,由于法规不同,请联系您当地的安全监管部门,获取相关条例。Super GelRed ® 还可以吸附到活性炭上做为化学废物处理。 |
| Super GelRed ® 检测下限是什么? | 一些用户反馈能够检测 0.1 ng 的 DNA 条带。但是,检测的极限还与仪器的灵敏度和曝光设置有关。 |
| Super GelRed ® 的结合机制是什 么? | Super GelRed ® 通过静电吸引的方式与 DNA 结合。 |
| Super GelRed ® 是否需要避光? | Super GelRed ® 是稳定的染料。你可以在室内光线下使用染料,但是我们建议染料保存时注意避光。 |
| 10000×Super GelRed ® in DMSO or water 之间是否有区别? | 水溶解的产品相对于用 DMSO 溶解的产品,是一个全新的改良。由于DMSO 会被皮肤吸收,我们建议染料溶于水,以避免 DMSO 的危害。鉴于有些用户不希望改变实验方案,我们将继续提供储存在 DMSO 中的染 料。 |

 爱康英文站
爱康英文站

